|
|
||
КТ-ангиография. Первый опыт применения.
Руцкая Е. А.1, Кавецкий С. И.2
1Белоруский государственный институт усовершенствования врачей, 2Республиканский Научно-практический Центр Детской Онкологии и Гематологии.
В последние годы в мировую практику широко внедряется КТ-ангиография, применение которой снижает потребность в выполнении рентгеноконтрастной ангиографии на 20-80% (в зависимости от анатомической области).
Разница показателей плотности кровеносных сосудов, окружающих их тканей и паренхиматозных органов в нативном изображении при КТ-исследовании несущественная.
Стандартная методика усиления КТ-изображения с в/венным введением водорастворимых
йодосодержащих контрастных веществ (0,5-0,8 мл/кг) с последующим сканированием
через 3-5 мин. фиксирует паренхиматозную фазу контрастирования органов
и не позволяет в достаточной мере дифференцировать сосудистые структуры.
Применение спиральной КТ, имеющей высокую скорость сканирования 0,5-1
см/сек, и синхронное в/венное введение контрастного агента со скоростью
1-3 мл/сек с помощью автоматического шприца-инъектора позволяет выполнить
КТ-ангиографию и визуализировать сосудистое русло на достаточном протяжении
на фоне окружающих органов и структур.
Контрастирование артериальных и венозных сосудов достигается путем выбора оптимального времени задержки между началом введения контрастного препарата и началом сканирования (выбор протокола КТА) , которое зависит в значительной мере от состояния гемодинамики, места инъекции, скорости введения препарата.
По результатам 1-ой Согласительной конференции по спиральной КТ , проведенной в ФРГ (1996), признано необходимым использование только неионных контрастных средств при КТ-ангиографии (иогексол, иопромид, иодиксанол и др.) с концентрацией йода 300-350 мг/м. При обычном протоколе КТА толщина среза составляет 5-10 мм, питч 1, скорость введения контрастного в-ва 1-2 мл/сек, объем введения примерно равен скорости введения, умноженной на общее время сканирования зоны интереса (обычно не более 100мл контрастного вещества).
Показаниями к применению КТА являются:
- аневризмы грудной и брюшной аорты (включая расслоения, разрывы, тромбозы);
- аномалии развития аорты и ее ветвей, легочной артерии;
- тромбоэмболии легочной артерии;
- стенозы и окклюзии почечных, подвздошных, бедренных, сонных артерий;
- аневризмы интракраниальных артерий;
- тромбы в крупных венах;
- опухоли с предполагаемой сосудистой инвазией или комирессией сосудов
для определения возможности и тактики оперативного вмешательства.
КТА сердца и коронарных артерий возможна на сверхбыстрых спиральных КТ (время среза меньше или = 0,1 сек).
В Республиканском научно-практическом центре детской онкологии и гематологии выполнено 37 КТ-ангиоргафий ( в 28 случаях детям от 1 до 15 лет) на спиральном компьютерном томографе Philips Tomoscan SR 4000 (время сканирования - 2 сек) с использованием автоматического инъектора СТ 9000 АДV.
Для определения взаимоотношений опухоли с крупными сосудами и возможности
оперативного вмешательства 13 пациентам контрастировались сосуды средостения
и шеи (Рис. 1-3).
КТА сосудов брюшной полости выполнена 24 пациентам для исключения инвазии
их опухолью забрюшинного пространства и почек. В 4 случаях был диагностирован
опухолевый тромб в нижней полой вене (НПВ)
(Рис. 4), в 9 случаях НПВ была окружена конгломератом опухоли
и л/узлов (Рис. 5).
|
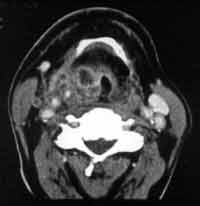
Рис. 1. КТА сосудов шеи у больного М., 55
лет раком гортани.
Увеличенные (метастазы) лимфоузлы в области бифуркации общей сонной артерии с компрессией внутренней яремной вены. Расширение поверхностной яремной вены, осуществляющей коллатеральный кровоток. |
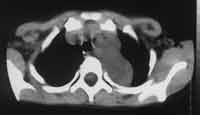 |
Рис. 2. Ганглионеврома верхнего средостения
у больной С., 10 лет.
(а) Нативное КТ-иследование, сосудистые элементы не дифференцируются в опухоли. |
|
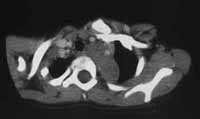
Рис. 2. Ганглионеврома верхнего средостения
у больной С., 10 лет.
(б) КТА артерий дуги аорты. Левая подключичная артерия расположена в толще опухоли, левая общая сонная артерия оттеснена кпереди. |
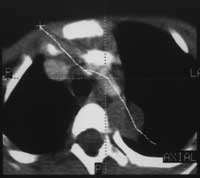 |
Рис. 2. Ганглионеврома верхнего средостения
у больной С., 10 лет.
(в) Кривая белая линия - плоскость реформации. |
 |
Рис. 2. Ганглионеврома верхнего средостения
у больной С., 10 лет.
(г) Реформация изображения контрастированных сосудов в плоскости дуги аорты. |
|
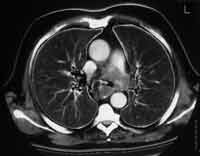
Рис. 3. Центральный рак легкого у больного К. , 53 года. КТА легочных артерий. Дефект контрастирования ствола и левой легочной артерии вследствие инвазии опухолью. |
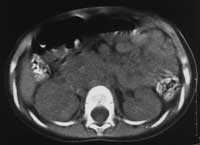 |
Рис. 4. Нефробластома правого надпочечника
у у б-го С., 1,5 лет.
(а) Нативное КТ-исследование. |
 |
Рис. 4. Нейробластома правого надпочечника
у б-го С., 1,5 лет.
(б) КТА. НПВ компремирована, располагается в толще опухоли. Сброс венозной крови в полунепарную вену. Деформация и отклонение правой почечной артерии. |
|
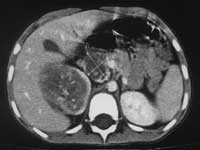
Рис. 5. Нефробластома справа у больной П.,
6 лет.
А-Б, С-Д – опухолевый тромб (дефект контрастирования) в просвете НПВ, контрастное вещество визуализируется в просвете сосуда тонкой пристеночной полоской (А). |
Основными преимуществами КТА в сравнении с “золотым стандартом”
- рентгеноконтрастной ангиографией являются:
- минимальная инвазивность метода - в/венная катетеризация при КТА
несравнимо безопаснее в/артериальной при стандартной АГ;
- КТА может выполняться амбулаторным пациентам;
- КТА позволяет оценить не только просвет, но и стенку сосуда, а также
взаимоотношения его с окружающими тканями и опухолью;
- при КТА возможно выполнение многоплоскостных и объемных реконструкцией
изображений (при соответствующем программном обеспечении), что значительно
облегчает интерпретацию и демонстрацию результатов исследования.
Таким образом, КТ-ангиография является высокоинформативным и относительно безопасным методом визуализации сосудов. Эффективность метода в определении взаимоотношений крупных сосудов и опухоли трудно переоценить.
Литература:
1. Терновой С. К. , Синицын В. Е.
Спиральная компьютерная и электронно-лучевая ангиография . М. : Bидар,
1998. 144 c.
2. Rogalla P. , Mutze S. , Hamm B. Body C. T. State-of-the-Art. - Munhen:
Zucksch werdt, 1996. 159 c.
|
||||||||